Verslag
Het mag dan nog geen tovermiddel zijn, maar de komende tien a vijftien jaar zullen stamcellen steeds vaker worden gebruikt om ziektes te genezen. Dat is de stellige overtuiging van stamcelbioloog en – onderzoeker Gerald de Haan (50) van het Universiteit Medisch Centrum Groningen. Hij praatte de bezoekers van het Kenniscafé bij over de laatste stand van zaken in de wondere wereld van de stamcel.
Zelf werkt De Haan bij Eriba, het instituut in Groningen dat het biologische proces van veroudering bestudeert. Mensen worden sinds 1850 steeds ouder, onder meer door veel betere hygiëne en de ontdekking van antibiotica. Inmiddels is kindersterfte zo sterk gedaald, dat de winst volgens De Haan nu vooral is te halen bij het tegengaan van verouderingsziektes. Waarbij cellen een grote rol spelen.
Want hoewel de wetenschap nog vol vragen zit, zijn een paar oorzaken van veroudering bekend. Bijvoorbeeld door schade aan het dna, ontstaan door ‘kopieerfouten’ van genetisch materiaal. Ook defecten aan eiwitten in cellen speelt een rol, bijvoorbeeld bij bekende ziekten als Alzheimer.
Maar terug naar stamcellen: wat zijn dat nu eigenlijk? Volgens De Haan bestaat een stamcel uit twee dochtercellen, waarvan er een identiek is aan de moedercel en de ander als het ware 'uitrijpt'. Ook deze cel schept weer twee dochtercellen: Dat proces gaat continu door, waardoor er steeds nieuwe cellen komen met dezelfde genetische eigenschappen.
Maar er is een belangrijk verschil tussen embryonale stamcellen – die in de eerste weken na de bevruchting worden aangemaakt – en ‘volwassen’ stamcellen. Alleen embryonale stamcellen kunnen namelijk nog tot alle types weefsel uitgroeien. Volwassen stamcellen daarentegen hebben als het ware al een opdracht gekregen om bijvoorbeeld een darmcel, huidcel of hartcel te worden. Deze adulte cellen kunnen dus eigenlijk maar een ding.
Wetenschappers mogen in Nederland geen menselijke embryonale stamcellen gebruiken, wel dierlijke. Die zou je buiten lichaam kunnen laten rijpen, om vervolgens de cel te gebruiken waarin je bent geïnteresseerd. Daar komen twee problemen bij kijken: hoe weet je welke ‘opdracht’ de cel in kwestie heeft gekregen en hoe kom je aan eenvoudig aan embryonale stamcellen?
Het laatste probleem is opgelost door de techniek, waardoor wetenschappers tegenwoordig niet afhankelijk zijn van een bevruchte eicel die uitgroeit tot een embryo. De oplossing is kloneren van dieren. In 1962 toonde de Britse wetenschapper John Gurdon al aan dat de specialisatie van een volwassen cel omkeerbaar is. Hij toonde dat aan door de kern uit een eicel van een kikker te halen en deze te vervangen door een cel uit het darmkanaal van een kikkervisje. Uit het eitje kwam een gezond kikkervisje.
Wat betreft de moeilijkheid om de ‘opdracht’ van een cel te achterhalen zorgde de Japanse wetenschapper Shinya Yamanaka in 2006 voor een doorbraak, die hem – samen met Gurdon – in 2012 de Nobelprijs opleverde. Hij ontdekte de vier eiwitten die een volwassen stamcel ‘programmeren’. Daardoor kan een volwassen stamcel weer worden teruggebracht naar het embryonale stadium, het stadium dus waarin een cel nog tot elk weefseltype kan uitgroeien. In theorie zouden van een patiënt dankzij deze techniek genetisch identieke donorcellen kunnen worden gekweekt. Daar wordt nu onderzoek naar gedaan. Ook loopt er ook onderzoek om met zulke donorcellen Macula degeneratie (aantasting van het netvlies) te verhelpen.
Zulke cellen zijn volgens De Haan overigens niet alleen van belang voor medische wetenschappers, maar ook voor de farmaceutische industrie. Die kan de werking van medicijnen op de cellen van een specifieke patiënt testen.
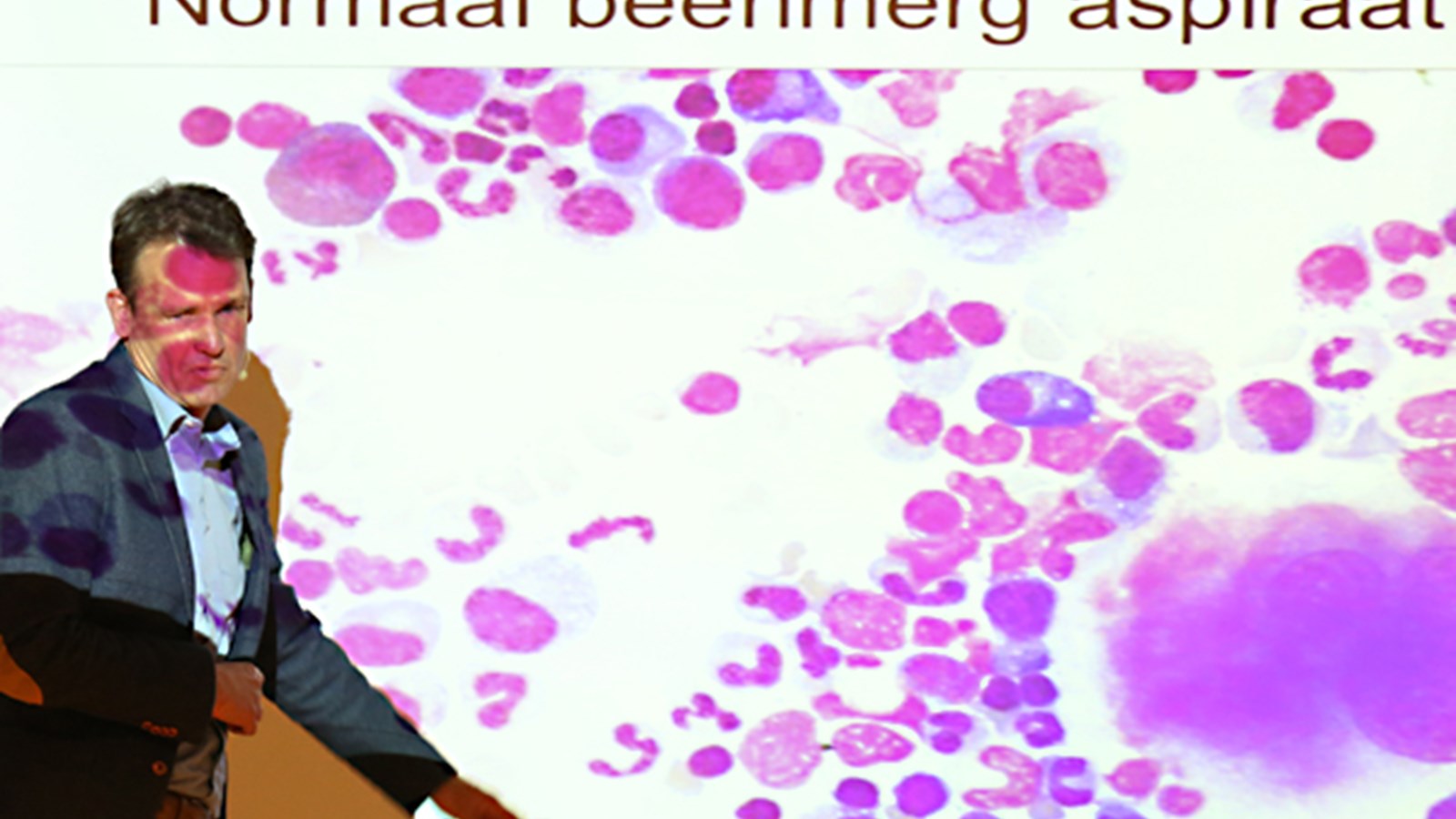
Vooralsnog worden stamcellen op grotere schaal vooral toegepast bij de bestrijding van defecten aan het immuunsysteem en van bloedziekten als leukemie. Bij die ziekte ontsporen stamcellen en gaan zich als een gek vermenigvuldigen. De behandeling bestaat er uit de slechte stamcellen te doden en te vervangen door gezonde donorcellen.
Die gezonde stamcellen worden vaak bij mensen in de directe omgeving van de patiënt gevonden, omdat de kans op genetische overeenkomsten dan het grootst is. Maar volgens De Haan kunnen mensen zich ook via de bloedbank als stamceldonor opgeven. In dat geval worden de gegevens in een internationale databank opgeslagen, waarin artsen naar een ‘match’ tussen patiënt en donor kunnen zoeken.